|
Классификация химических реакций
Тема: Классификация химических реакций.
Что нужно знать:
Явления, происходящие с веществами можно разделить на физические и химические:
Химические явления (реакции)
|
Физические явления
|
Происходит превращения одних веществ в другие. Появляются новые вещества с новыми свойствами.
|
Не происходит образования новых веществ, а меняется форма или агрегатное состояние. Обратимы.
|
Горение веществ
Скисание молока
Растворение металла в кислотах
|
Измельчение веществ
Плавление, затвердевание или испарение веществ
Растворение сахара, соли в воде
|
Признаками химической реакции являются:
-изменение цвета,
-появление запаха,
-выделение газа;
-образование нерастворимого осадка;
-выделение тепла (иногда и света).
Химическим уравнением называется условная запись химической реакции с помощью химических формул и коэффициентов. Число атомов одинаковых элементов в левой и правой части уравнения должны быть равны.
По числу веществ до и после реакции химические реакции подразделяют на :
Соединение
|
Разложение
|
Замещение
|
Обмен
|
А + В = С
|
А = В + С
|
А + ВС = АС + В
|
АВ + СD = АD + СВ
|
O2 + 2H2 = 2H2O
|
CaCO3 = CaO + CO2
|
Zn + 2HCl =
ZnCl2 + H2
|
ZnO + H2SO4 =
ZnSO4 + H2O
|
По тепловому эффекту реакции классифицируют на:
Экзотермические
|
Эндотермические
|
Идут с выделением тепла.
|
Идут с поглощением тепла
|
С + О2 = СО2 + Q
|
CaCO3 = CaO + CO2 – Q
|
Реакции соединения являются экзотермическими, реакции разложения – эндотермическими. Реакции нейтрализации (кислота + основание) идут с выделением тепла.
По направленности процесса реакции классифицируют на:
Необратимые
|
Обратимые
|
Протекают в одном направлении и заканчиваются, когда израсходуется один из реагентов
|
Идут как в прямом, так и в обратном направлении
|
Zn + 2HCl = ZnCl2 + H2
|
N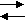 2 + 3H2 2 NH3 2 + 3H2 2 NH3
|
По наличию границы раздела между веществами реакции классифицируют на:
Гомогенные
|
Гетерогенные
|
Отсутствует поверхность раздела между взаимодействующими веществами. Реакция протекает во всем объёме. Это реакции между газообразными веществами, реакции в растворах.
|
Вещества отделены друг от друга поверхностью раздела. Реакция протекает на поверхности твердого вещества.
|
H2 (г) + Cl2 (г) = 2 HCl
NaOH (p-p) + HCl (p-p) = NaCl + H2O
|
Zn (тв) + H2SO4 (р-р) = ZnSO4 + H2
С (тв) + О2 (г) = СО2
|
По наличию катализатора реакции классифицируют на:
Каталитические
|
Некаталитические
|
Катализаторы – это вещества, которые изменяют скорость реакции, но сами не расходуются в результате её протекания.
Химические реакции, которые протекают в присутствии катализатора, называют каталитическими
|
Химические реакции, протекающие без катализатора
|
кат
N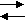 2 + 3H2 2 NH3 2 + 3H2 2 NH3
|
NaOH + HCl = NaCl + H2O
|
По изменению степеней окисления реакции классифицируют на:
Окислительно-восстановительные (ОВР)
|
Не ОВР
|
Идут с изменением степени окисления элементов
|
Степени окисления элементов не изменяются
|
Zn0 + H2+SO4 = Zn+2SO4 + H20
|
Ca+2C+4O3-2 = Ca+2O-2 + C+4O2-2
Na+O-2H+ + H+Cl -= Na+Cl -+ H2+O-2
|
Все реакции обмена – не ОВР.
Пример задания:
Какое из указанных уравнений соответствует реакции обмена?
Mg + CuSО4 = MgSО4 + Сu
CaO + СО2 = CaCО3
AgNО3 + NaCl = AgCl + NaNО3
Zn(OH)2 = ZnO + H2О
Решение: Реакцией обмена называют реакцию между сложными веществами, в результате которой образуются два новых сложных вещества.
замещение
соединение
обмен
разложение
Верный ответ – 3.
Ещё пример задания:
К химическим явлениям относится процесс
1) измельчения сахара до состояния пудры
2) превращение воды в лед
3) появление капель воды на крышке чайника
4) горение свечи
Решение:
при измельчении сахара не появляется нового вещества – физическое явление;
переход воды в твердое состояние – физическое явление;
испарение и конденсация воды – физическое явление;
при горении свечи образуются пары воды и углекислый газ, выделяется свет и тепло – химическое явление
Верный ответ – 4.
Ещё пример задания:
Уравнением химической реакции является запись:
4P + 5O2 = 2P2O5
NaOH + H2SO4 = Na2SO4 + H2O
P + Cl2 = PCl5
Fe2O3 + HCl = FeCl3 + H2O
Решение:
Только в первой реакции с помощью коэффициентов уравнено число атомов до и после реакции, остальные являются не уравнениями, а схемами реакций.
Верный ответ – 1.
Ещё пример задания:
Сумма коэффициентов в уравнении реакции между оксидом калия и соляной кислотой равна
1) 5 2) 6 3) 7 4) 4
Решение:
Составим уравнение реакции:
K2O + 2HCl = 2KCl + H2O
Сумма коэффициентов равна 1 + 2 + 2 + 1 = 6
Верный ответ - 2
Ниже приведены задания для тренировки.
Ответы к заданиям:
Зада-ние
|
1
|
2
|
3
|
4
|
5
|
6
|
7
|
8
|
9
|
10
|
11
|
12
|
13
|
14
|
15
|
16
|
17
|
18
|
19
|
20
|
ответ
|
1
|
1
|
2
|
2
|
4
|
3
|
4
|
4
|
3
|
2
|
3
|
3
|
4
|
3
|
3
|
2
|
1
|
1
|
3
|
4
|
Химические реакции.
Задания для тренировки:
Признаком химической реакции является:
выделение энергии
изменение формы тела
изменение агрегатного состояния
уменьшение размеров частиц
Какое уравнение соответствует реакции соединения?
Na2O + H2O = 2 NaOH
2HCl + MgO = MgCl2 + H2O
2AgNO3 = 2Ag + 2 NO2 + O2
H2SO4 + Fe = FeSO4 + H2
3) К реакциям замещения относится взаимодействие между
1) аммиаком и хлороводородной кислотой
2) цинком и раствором сульфата меди (II)
3) раствором гидроксида натрия и оксидом серы (VI)
4) серной кислотой и хлоридом бария
4) К физическим явлениям относят
1) скисание молока
2) засахаривание варенья
3) горение свечи
4) пригорание пищи
5) Какое уравнение соответствует реакции замещения?
1) NH3 + HNO3 = NH4NO3
2) H2S + MgO = MgS + H2O
3) SO3 + 2NaOH = Na2SO4 + H2O
4) CuO + H2 = Cu + H2O
6) В уравнении химической реакции, схема которой
Fe2O3 + CO = Fe + CO2
коэффициент перед формулой угарного газа равен
1) 1 2) 2 3) 3 4) 6
7) К реакциям обмена относят реакцию, уравнение которой
1) CaO + SO3 = CaSO4
2) 2Na + 2H2O = 2NaOH + H2
3) 2Al(OH)3 = Al2O3 + 3H2O
4) H2S + 2KOH = K2S + 2H2O
8) Какая запись соответствует уравнению реакции горения фосфора?
1) Р + О2 = Р2О5
2) Р + 5О2 = 2 Р2О5
3) 4Р + О2 = 2 Р2О5
4) 4Р + 5О2 = 2 Р2О5
9)Какое уравнение соответствует реакции обмена?
SO2 + O2 = 2SO3
2Na + 2H2O = 2NaOH + H2
HCl + NaOH = NaCl + H2O
2Al(OH)3 = Al2O3 + 3H2O
10)Какое уравнение соответствует реакции соединения?
2HCl + Ca(OH)2 = CaCl2 + 2H2O
NH3 + HNO3 = NH4OH
2H2S + 3O2 = 2SO2 + 2 H2O
CuO + H2 = Cu + H2O
11) К физическим явлениям относится процесс
пожелтения листьев деревьев
ржавления чугунной ограды
деформации пластмассы
позеленения медных памятников
12) Химической реакцией является
получение кислорода перегонкой жидкого воздуха
растворение кислорода в воде
получение кислорода из перманганата калия
сжижение газообразного кислорода
13) Какое уравнение соответствует реакции разложения?
Cu + Hg(NO3)2 = Cu(NO3)2 + Hg
4NO2 + 2H2O + O2 = 4 HNO3
2HCl + MgO = MgCl2 + H2O
(NH4)2CO3 = 2 NH3 + CO2 + H2O
14) К химическим явлениям относится процесс
образование кристаллов сахара при длительном хранении варенья
растворение кислорода в воде
получение кислорода из перекиси водорода
сжижение газообразного азота
15) К окислительно-восстановительным относят реакцию
2Fe(OH)3 = Fe2O3 + 3 H2O
2) NH4Cl = NH3 + HCl
3) 2Cu(NO3)2 = 2CuO + 4NO2 + O2
4) H2SiO3 = SiO2 + H2O
16) К физическим явлениям относится процесс
обугливания древесины
2) плавления парафина
3) разложения мрамора
4) растворения аммиака в воде
17) Какое уравнение соответствует реакции замещения?
2K + 2H2O = 2KOH + H2
2) 2Al(OH)3 = Al2O3 + 3 H2O
3) CH4 + 2 O2 = CO2 + 2 H2O
4) 2KNO3 = 2KNO2 + O2
18) Сумма коэффициентов в уравнении реакции между оксидом натрия и оксидом фосфора (V) равна
1) 6 2) 7 3) 9 4) 10
19) К химическим явлениям относится процесс
1) образования инея
2) плавление парафиновой свечи
3) горения древесины
4) распространение запаха духов
20) Какая из записей соответствует уравнению окислительно-восстановительной реакции?
1) CO2 + Ca(OH)2 = CaCO3 + H2O
2) 2HBr + Na2O = 2NaBr + H2O
3) H2SO4 + BaO = BaSO4 + H2O
4) 2NO2 + H2O = HNO3 + HNO2 |
|
|
 Скачать 83.54 Kb.
Скачать 83.54 Kb.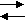 2 + 3H2 2 NH3
2 + 3H2 2 NH3