Биогеохимические циклы элементов
 Скачать 235.85 Kb. Скачать 235.85 Kb.
|
                МОУ МОУСпасская общеобразовательная средняя школа Реферат На тему: «Биогеохимические циклы элементов» Выполнила: Ученица 9 «Б» класса Рыжова Ксения Руководитель: Судницына Г. В. СОДЕРЖАНИЕ.
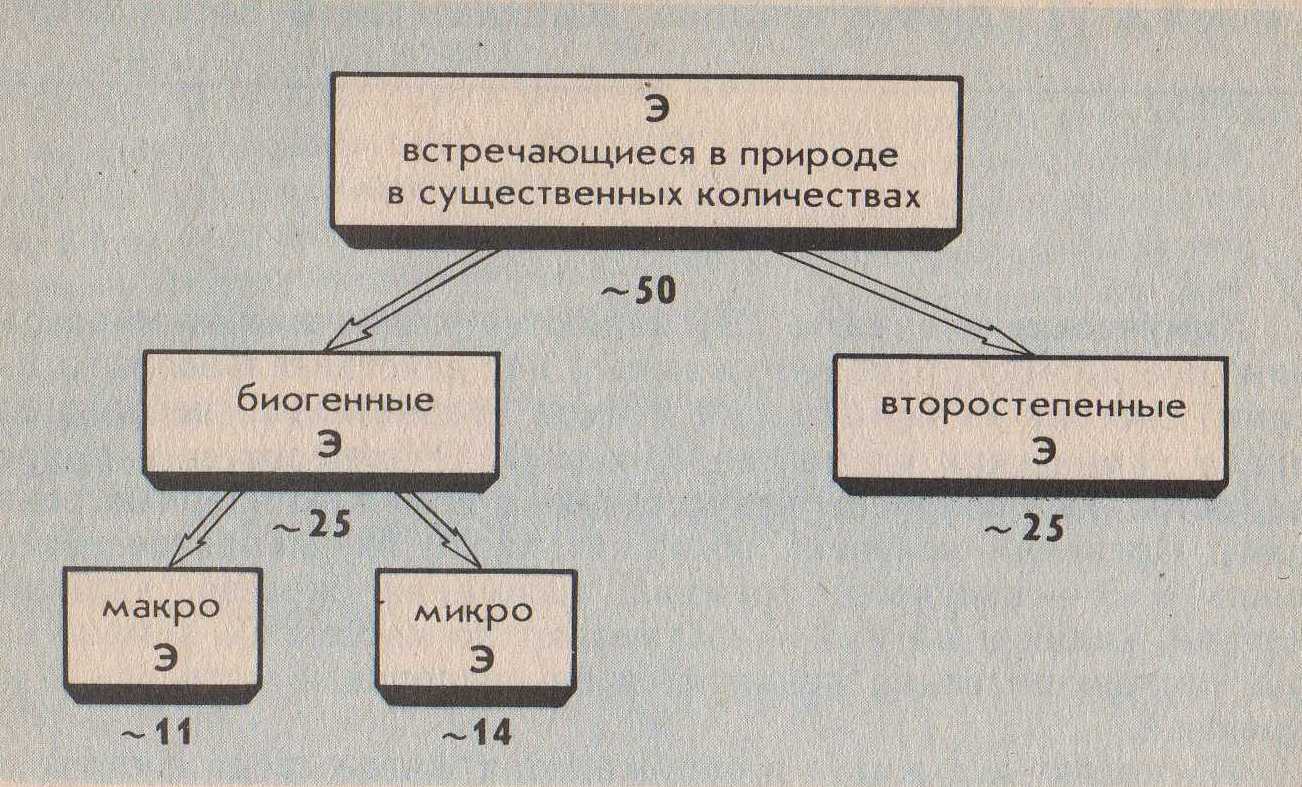
1.Химические элементы (Э). Являются кирпичиками мироздания. Всё многообразие окружающей нас действительности (и мы сами) состоит из комбинаций атомов сравнительно небольшого числа химических элементов. Около 90 Э существует в природе (остальные получены искусственно с помощью ядерных реакций). Организм человека содержит около 70 элементов. Всего лишь 8 Э – кислород, кремний, алюминий, железо, кальций, натрий, калий и магний – составляют по массе 99% земной коры, причём половина приходится на кислород, а четверть – на кремний. Поскольку всё живое и окружающая среда состоят из атомов определённых элементов, совершенно ясно, что любое экологическое взаимоотношение только тогда будет глубоко раскрыто и понято, когда будут проанализированы атомно-молекулярные основы этого взаимоотношения. Циклические перемещения химических Э в биосфере придают последней определённую стабильность и обусловливают её специфические свойства. Поэтому рассмотрение вопросов превращения Э в природе, роли, которую они играют для биосферы, её живых и неживых компонентов является ключевым моментом для понимания основ той или иной экологической проблемы. 2.Элементы биогенные и "второстепенные". Из химических элементов, встречающихся в природе в существенных количествах (а таких ≈ 50), примерно половину составляют биогенные элементы. Они жизненно необходимы организмам. Оставшаяся половина – "второстепенные" Э, не представляющие какой-либо известной ценности для живой клетки (приложение 1). Сам термин "второстепенные элементы" не совсем удачен. В природе нет таких элементов, к которым можно бы было относиться пренебрежительно. "Второстепенность" значит – редкость, слабое распространение атомов некоторых элементов в составе живой природы. В свою очередь, биогенные Э делятся на макро- и микроэлементы (приложение 1а). 3. Макро- и микроэлементы. Макроэлементы (у животных к ним обычно относят 11 Э) включают две группы: основные (6), из которых строятся биомолекулы клетки – белки, нуклеиновые кислоты, липиды и углеводы, и другие(5). Для углерода, азота, кислорода и водорода используют также исторически сложившееся общее название органогены – т.е. элементы, порождающие органические вещества. Роль микроэлементов в жизни человека для одних из них доказана, для других вероятна. Главный критерий, по которому отличают макро- от микроэлементов – потребность организма в элементе (выраженная в мг/ кг массы или мг/ сутки). Ежедневная потребность в макроэлементах составляет примерно 100 мг/сутки, тогда как в микроЭ не превышает нескольких миллиграммов (приложение 1а). Макро- и микроэлементы имеют и другие различительные особенности. Так, содержание макроэлементов в организме находится на постоянном уровне и даже случайные существенные отклонения от этого уровня не вызывают серьёзных осложнений для жизни. Недостаток или избыток микроэлементов (даже незначительный) приводит к заболеваниям. Другая особенность макро- и микроэлементов заключается в том, что первые в организме представлены в основном органическими соединениями (прежде всего это относится к основным макроэлементам), в то время как вторые входят в состав сравнительно простых неорганических или координационных (комплексных) соединений. Хочу заметить, что питательной ценностью обладают лишь биологически доступные Э, которые содержатся в пищевых продуктах в виде солей или других растворимых химических соединений. Макро- и микроэлементы не всегда удаётся чётко разграничить, особенно если это деление применять к разным группам организмов. Так, для растений набор микроэлементов (приложение 2) несколько отличен от такового набора для животных: бор, например, необязателен для последних, а натрий не столь существенен для растений. Для некоторых микроорганизмов бор крайне необходим: при его недостатке в почве клубеньковые бактерии, например, перестают фиксировать азот и питаются за счёт растений. Т.о. биогенные Э являются основными компонентами биосферы. 4.Содержание химических элементов в биосфере и теле человека. В живые организмы атомы элементов попадают из окружающей среды и после различных превращений и определённого времени пребывания в них возвращаются вновь в среду. При таком подходе живые организмы можно назвать открытыми системами (с точки зрения термодинамики), т.е. свободно обменивающимися с внешним миром веществом и энергией. Нахождение того или иного Э в организме и доля его в последнем определяются в основном следующими факторами: -наличием Э в природе в доступной (чаще всего водорастворимой) форме; -способностью организма поглощать Э; -способностью организма удерживать (накапливать) Э в своём теле. (приложение 2а) 5. Биогенные элементы – связующее звено между живой и неживой компонентами экосистем. Экосистема – единый комплекс, образованный живыми организмами и средой их обитания, в котором живые и неживые компоненты обмениваются между собой веществами и энергией. Химические элементы в экосистемах циркулируют (т.е. совершают круговорот), причём обмен элементами между составными частями экосистемы сбалансирован (приложение 3). Например, круговорот углерода и кислорода обеспечивается взаимодополняющими (комплементарными) процессами фотосинтеза и дыхания: ФОТОСИНТЕЗ nCO2+nH2O+E→ (CH2O)n+nO2 углеводы ДЫХАНИЕ (CH2O)n+nO2→ nCO2+nH2O+E углеводы Процессы дыхания представляют собой по химической сути реакции окисления созданных продуцентами органических веществ. При этом извлекаются запасённая в химических связях этих веществ энергия Е, которая, в свою очередь, переводится форму АТФ – аденозинтрифосфорной кислоты. В этой удобной форме Е легко хранится в клетке и столь же легко извлекается на осуществление движения, роста, развития, размножения и прочих функций живого. Т.о., общий путь Е в экосистемах однонаправлен (от Солнца через зелёные растения-автотрофы к животным-гетеротрофам) и связан с неизбежными потерями в форме теплоты (приложение 3а). Однако на планете существуют организмы, которые, создавая сами необходимые им в качестве пищи органические вещества, обходятся без солнечной энергии. Это хемосинтезирующие бактерии. Сам же процесс "бессолнечного" синтеза органических веществ, осуществляемый ими, получил название хемосинтеза (от греч. хемия – химия + синтез – соединение). Его открыл в 1887 году русский микробиолог С.Н.Виноградский (1856-1953). Необходимую энергию хемосинтезирующие микроорганизмы получают, окисляя неорганические соединения(NH3, H2, H2S, Fe S2 и т.д.), во внутриклеточных экзотермических реакциях. Хемосинтезирующих бактерий называют, поэтому еще и хемотрофами (чтобы отличить от гелиотрофов – зелёных растений). Примерами хемотрофов являются серобактерии, играющие одну из центральных ролей в круговороте серы. Большинство серобактерий окисляют серу (равно как H2 S или тиосульфат – ионы S2 О3²ˉ). Роль окислителя при этом могут выполнять нитрат-ионы: 5S+6NO3ˉ+ 2H2O→5SO4²ˉ+3N2+4H В этом процессе на 1 моль окисляемой серы выделяется 546 кДж энергии. Другие важнейшие хемотрофы-нитрификаторы, окисляющие в две стадии аммиак до азотной кислоты. Первую стадию осуществляют бактерии рода Nitrozomonas: 2 NH3+3O2→2HNO2+2H2O+660 кДж Азотистую кислоту окисляют до азотной бактерии рода Nitrobacter: 2 HNО2+O2→2HNO3+158 кДж Хемотрофы, т.о., отличаются от фотографов лишь источниками энергии, которую они используют на построение органических молекул. Хемотрофы заслуживают того, чтобы обратить на них особое внимание. Именно они впервые в истории развития жизни в условиях первобытной Земли научились использовать энергию превращения химических соединений для своих жизненных нужд. Потоки элементов питания и энергии от одного организма к другому в экосистемах составляют пищевую цепь (приложение 4). В реальности в экосистемах пищевые цепи переплетены, образуя сложную структуру трофических взаимосвязей всех обитателей данной экосистемы. Такую структуру называют пищевой сетью. Таким образом, биогенные элементы выполняют роль связующего звена между биотическими и абиотическими компонентами экосистем. 6.Блочная модель круговорота биогенных элементов в природе. Экосистему более детально можно представить в виде пяти блоков (три активных, два добавочных), через которые проходят различные вещества (Приложение 4а). Три активных блока составляют обменный фонд элементов (Приложение 3а): -живые организмы; -мёртвый органический детрит (от лат. детритус-истертый); -доступные неорганические вещества. Два добавочных блока составляют резервный фонд элементов: -косвенно доступные неорганические вещества; -осаждающиеся органические вещества. Между активными блоками идёт быстрый обмен элементами. Обмен между добавочными блоками и остальной частью экосистемы замедлён. Наиболее значительные (весомые) процессы в круговороте элементов в приложении 4а выделены жирными стрелками, что означает непрерывность обмена в экосистеме биогенными элементами. 7.Биогеохимические циклы элементов. Как же происходит обменный круговорот? Биогенные элементы, как уже было отмечено, циркулируют в экосистеме, т.е. совершают биогеохимические циклы. Термин "биогеохимический цикл" ввёл в обиход В.И.Вернадский. Все биогеохимические циклы взаимосвязаны в природе и в совокупности формируют устойчивую структуру биосферы в целости. Замкнутость нормальных биогеохимических циклов неполная – и это очень важное свойство. Именно оно обусловило биогенное накопление кислорода и азота в атмосфере Земли, а также различных химических элементов и их соединений в литосфере. Вместе с тем следует иметь в виду, что доля вещества выходящего из биосферного цикла (длительностью от десятков и сотен до нескольких тысяч лет) в геологический цикл (длительностью в миллионы лет), в год относительно невелика. Лишь громадное время истории развития биосферы (около 4 млрд. лет) позволило осуществить подобные биогенные накопления элементов в атмосфере и литосфере. Так, например, ежегодный сброс углерода из биогеохимического цикла наземных экосистем в геологический цикл составляет около 130 т, т.е. всего лишь примерно10-8 % от современных запасов углерода, находящихся в биосферном обращении. В палеозое за счёт неполной обратимости цикла углерода накопились мощные запасы отложений – известняки, уголь, нефть, битумы и пр., т.е. примерно за 600 млн. лет 10161017т. В каждом биогеохимическом цикле (т.е. для каждого отдельного элемента) можно выделить два фонда (приложение 3а, 4а). 1. Резервный – большая масса медленно движущихся веществ, содержащих данный элемент, в основном в составе абиотического компонента. В приложении 6 этот фонд обозначен буквой Э в кружке. Фонд размещён за пределами живых организмов, во внешней среде. 2. Обменный (подвижный) – меньший фонд, но более активный. Для него характерен быстрый обмен между организмами и их непосредственным окружением. В приложении 5 представлен пищевой сетью и стрелками от резервного фонда. Резервный фонд иногда называют недоступным, а обменный циркулирующий фонд – доступным, хотя между ними существует постоянный медленный обмен. Среди биогеохимических циклов выделяют циклы двух типов: газообразных и осадочных веществ (Приложение 5а). Такое деление – проявление склонности химических элементов образовывать соединения того или иного типа в условиях Земли. Циклы функционируют под действием биологических и геологических факторов. Существование биогеохимических циклов создаёт возможность для саморегуляции системы, что придаёт экосистеме устойчивость – постоянство состава (в %) различных элементов в гомеостазе. В связи с хозяйственной деятельностью человека и вовлечением в биосферный поток техногенных продуктов этой деятельности возникли проблемы, обусловленные нарушением природных биогеохимических циклов. Циклы некоторых элементов (например, азота, серы, фосфора, калия, тяжёлых металлов) превратились в настоящее время в природно-антропогенные, характеризующиеся значительной незамкнутостью. Некоторые же соединения и материалы, созданные человеком (например, многие пластмассы), вообще не способны включаться в природные и природно-антропогенные циклы, т.к. не перерабатываются в экосистемах, загрязняя их и являясь абсолютно чуждыми живому веществами. И сейчас задача человека в содействии возвращения веществ и элементов в круговорот. 8.Круговорот азота в биосфере. Цикл азота служит примером сложного круговорота газообразных веществ, способного к быстрой саморегуляции. Азот наиболее распространён на Земле в форме газообразного N2 атмосферы. И хотя азот - важнейший компонент белков и нуклеиновых кислот генетического материала живых организмов), растения не могут непосредственно брать его из атмосферы. Они способны усваивать лишь связанный с кислородом или водородом азот, т.е. переведенный в другие химические формы – аммиак NH3 , ионы аммония NH4 или нитрат-ионы NO3 (Приложение 6). Процесс связывания атмосферного азота некоторыми свободноживущими (род Azotobacter) и симбиотическими (род Rhizobim) бактериями – азотфиксаторами называют биологической фиксацией азота. Каждый год таким путём на Землю переносится примерно 17,5*1010 азота. Фермент нитрогеназа, "обслуживающая" у бактерий функцию N2 , зависит в своей активности от присутствия микроэлемента молибдена. Т.о. наблюдается тесное взаимодействие макро- и микроэлементов в биогеохимическом цикле азота. 9.Круговорот фосфора в биосфере. Главным резервуаром фосфора (в отличие от азота) служит не атмосфера, а горные породы прошлых геологических эпох. К растениям фосфор попадает главным образом в виде фосфатов (Приложение 6а). Соединения фосфора растворимы лишь в кислых растворах и в таком виде пригодны для усвоения растениями. В щелочных растворах и кислородной среде фосфор связан обычно в нерастворимые соединения с кальцием, например в составе апатитов 3 Са3 (РО4)2 *Са (Сl, F) 2 и фосфоритов Са 3 (РО4)2. Незначительное количество фосфора возвращаются из воды на сушу благодаря рыболовству, а также с экспериментами морских птиц. Однако в целом поток фосфора идёт в одном направлении - из наземных горных пород на дно моря. Из всех макроэлементов Р - один из самых дефицитных. Фосфор заслуживает особо пристального внимания в связи с тем, что роль его истории развития жизни на Земле трудно переоценить. Будучи относительно редким элементом (9*10-2 % от массы всей земной коры), фосфор тем не менее лежит в основе уникальной системы снабжения живых организмов энергией! Для того чтобы на древней Земле затеплилась жизнь, потребовалась особая форма энергии, поддерживающая эту жизнь, - энергия фосфатных ( или, как их называют иначе, фосфоангидридных) Р – О – Р – связей. Простейшим представителем таких " энергонесущих " молекул является пирофосфат: О О О ║ ║ ║ Н4Р2О7→НО―Р―О―Р―ОН+Н2О→2НО―Р―ОН+29 кДж │ │ │ ОН ОН ОН 2 Н3 РО4 При гидролизе пирофосфата высвобождается энергия (более 29 кДж/моль), что значительно больше, чем если бы гидролизу подвергалась любая другая молекула, не содержащая Р – О – Р – связей. Для организмов роль главного источника энергии играет другое соединение, имеющее фосфоангидридные связи. – знаменитая аденозинтрифосфорная кислота – АТФ. Роль АТФ в жизни клетки сравнивают с ролью денег в хозяйстве. Клетка "расплачивается" этим соединением за всё, что ей необходимо. Многие ферменты (белки-катализаторы биохимических реакций) используют энергию АТФ. С помощью АТФ клетка движется, вырабатывает теплоту, избавляется от отходов, синтезирует новые вещества. В молекуле АТФ есть две высокоэнергетические (макроэргические) Р – О – Р – связей . Их обычно изображают волнистыми линиями. Разрыв их (например, при гидролизе) освобождает значительное количество энергии. Термин "макроэнергическая" относит к таким ковалентным связям, разрыв которых сопровождается выделением энергии не менее 29 кДж/моль. Т.о., в известную фразу: "Земная жизнь сформировалась на основе углерода" – можно смело добавить "и фосфора". 10.Круговорот углерода в биосфере. Круговорот углерода осуществляется благодаря чётко отлаженному в ходе эволюции механизму функционирования двух фундаментальных процессов. Солнечная энергия в форме электромагнитного излучения используется биосферой при фотосинтезе. Последний представляет собой весьма сложный с химической точки зрения процесс, который может осуществлять лишь те организмы, в клетках которых работают уникальные молекулы хлорофилла. В процессе фотосинтеза электромагнитная энергия Солнца переходит в энергию химических связей органических соединений, прежде всего углеводов (СН2О)n. Клеточное дыхание – противоположные фотосинтезу процесс, в котором происходит расщепление синтезированных из СО2 и Н2О углеводов. Цель его – извлечь энергию из молекул углеводов (путём окисления), перевести её в форму АТФ и далее использовать на различные энергетические нужды клетки. Выделяемый при фотосинтезе О2 все организмы (и животные-гетеротрофы, и растения-автотрофы) используют для окисления (СН2О)n. Фотосинтетическая активность наземных растений, бактерий и морских водорослей приводит к фиксации углерода из атмосферы и воды и внедрению его в состав органического вещества. Циклическими путями этот углерод попадает в клетки животных и микроорганизмов. Окисляя органические вещества, живые клетки возвращаются СО2 в атмосферу и воду. Тот же фокус "возвращения палеозойского СО2" в атмосферу проделывает человек, сжигая уголь или нефть (Приложение 7). Т.о., цикл углерода (Приложение 7) с глобальной точки зрения – сложный биосферный процесс, объединяющий в единое понятие "жизнь, живое" все отдельные организмы, населяющие планету. 11.Второстепенные элементы в биосфере. Стронций-90. Цезий-137. Ртуть. Радиоактивный стронций-90 крайне опасен для человека и других позвоночных. Если раньше это был совершенно игнорируемый экологами элемент, то сейчас – объект особого внимания в связи с тем, что он по химическим свойствам родствен кальцию и, попав в организм, легко накапливается в костях и контактирует с кровью (Приложение 7а). Стронций-90 – один из продуктов расщепления урана с большим периодом полураспада. Его источники – ядерные взрывы и работающие АЭС. Хотя эти источники дают ничтожные количества стронция-90, последний, попадая в осадки и мигрируя вместе Са2+ из почвы и воды в растения, животных и пищу, человека, способны накапливаться в костях до угрожающих жизни концентраций. Другой опасный продукт деления атомного ядра – радиоактивный изотоп цезий-137 – схож по свойствам с биогенным калием и поэтому также способен быстро включаться в цикл последнего, циркулируя вместе с ним по пищевым цепям. А ведь он – канцероген (от лат. канцер – рак). Эти два элемента (точнее, их радиоактивные изотопы) – примеры "нового вещества" в биосфере, т.е. такого, которого не существовало до появления человека (или его количества в биосфере были ничтожно малы и не оказывали никакого влияния не развитие последней). Именно деятельность человека способствовала активному вовлечению опасных второстепенных элементов в биосферные циклы. Ещё один пример элемента, загрязняющего окружающую среду исключительно с помощью человека, - ртуть Нg (Приложение 8). До индустриальной эры ртуть не оказывала на жизнь организмов практически никакого действия, т.к. её концентрация в природе мала и подвижность в биосфере низка. Ртуть – чрезвычайно токсичный элемент (как сам металл, так и его соединения). Особенно опасны для живого органические производственные ртути, такие, например, как ион метилртути CH3Hg+ и диметилртуть (CH3)2Hg. К большому несчастью, процесс образования этих форм ртути идёт в природе и без участия человека, точнее сказать, вслед за его деятельностью. Некоторые микроорганизмы способны метилировать те формы ртути, которые оставил после себя человек. 12.Заключение. Завершая разговор о биогеохимических циклах элементов, необходимо подчеркнуть следующие особо важные моменты:
 ПРИЛОЖЕНИЕ 1 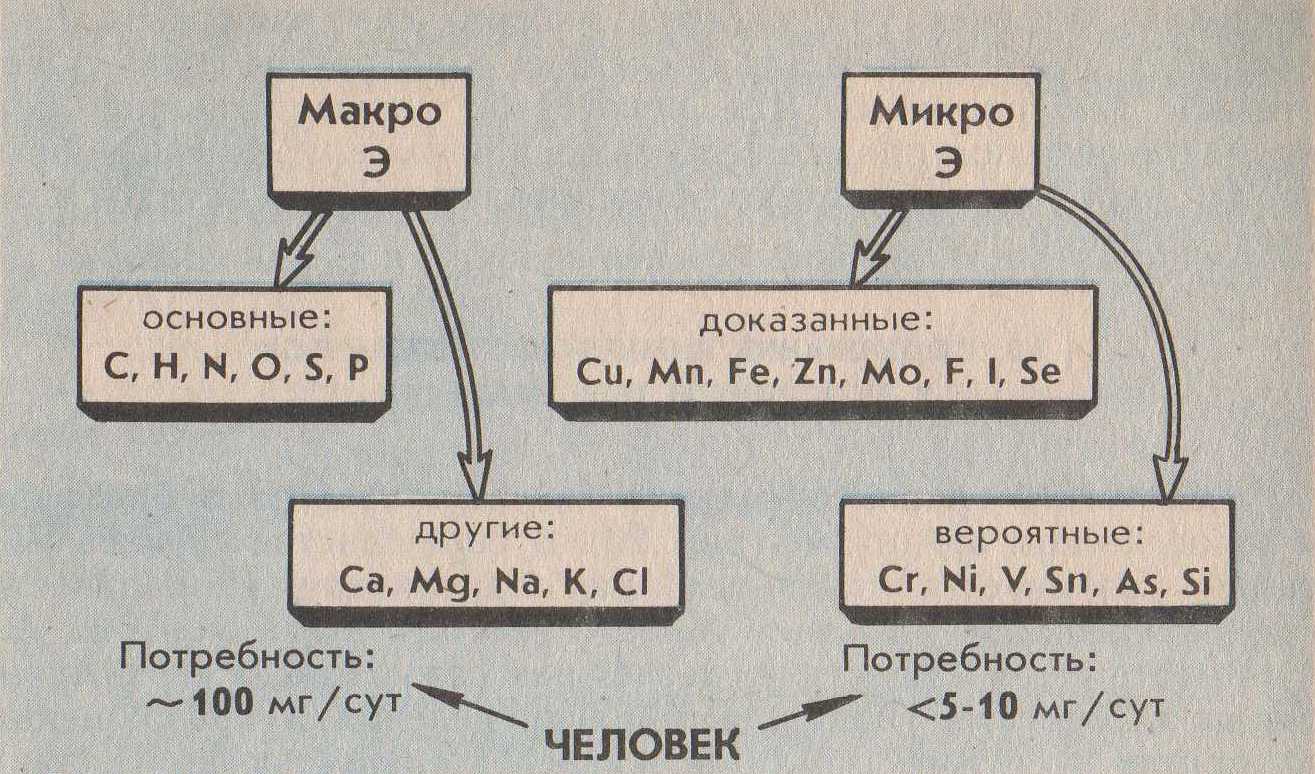 ПРИЛОЖЕНИЕ 1А 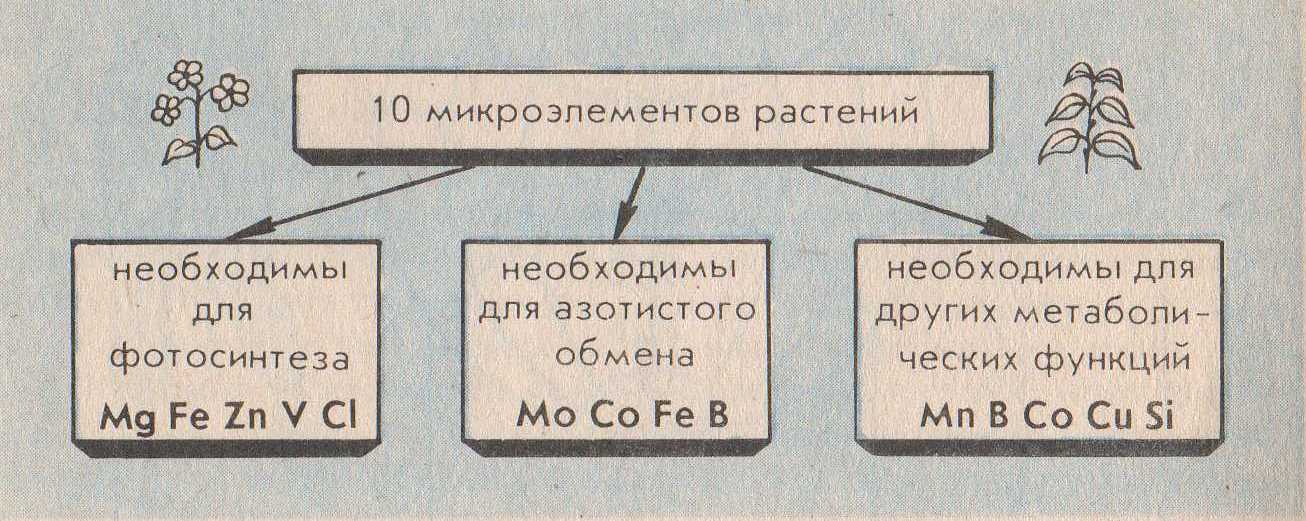  ПРИЛОЖЕНИЕ 2 ПРИЛОЖЕНИЕ 2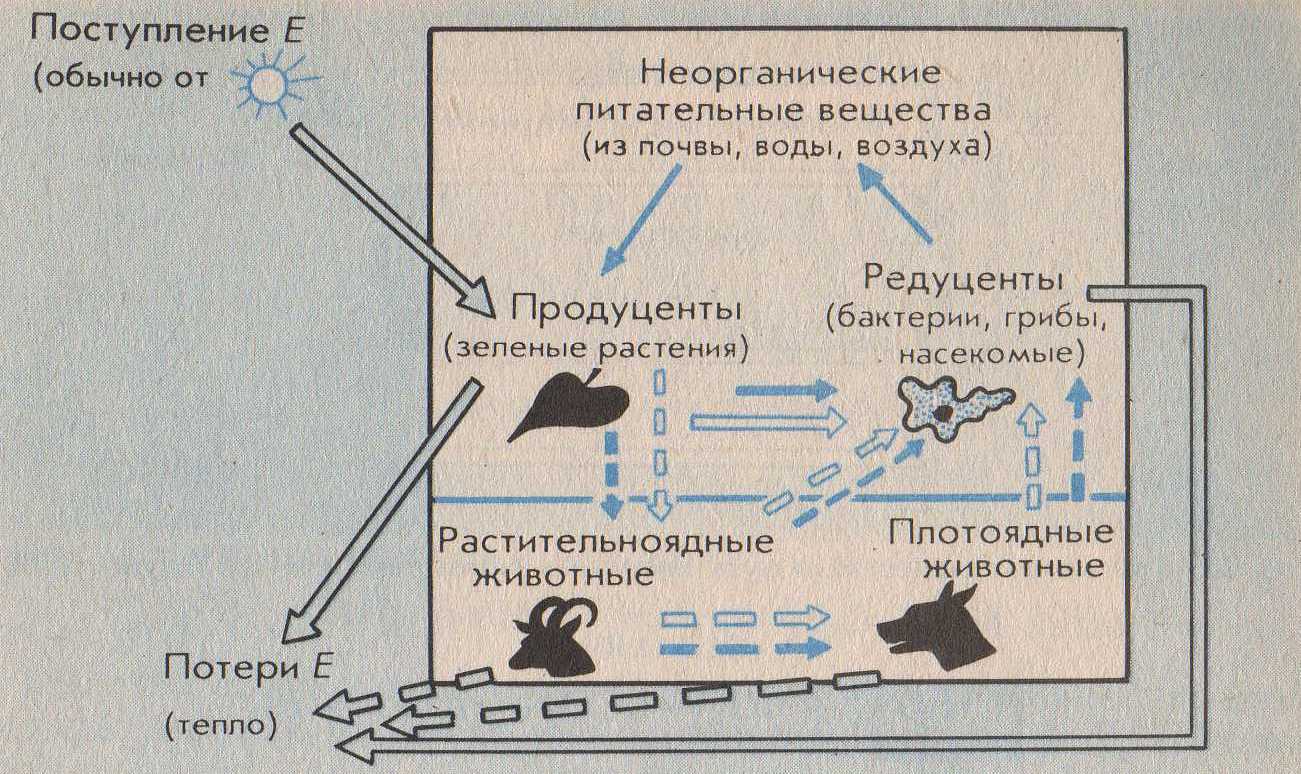 ПРИЛОЖЕНИЕ 2А 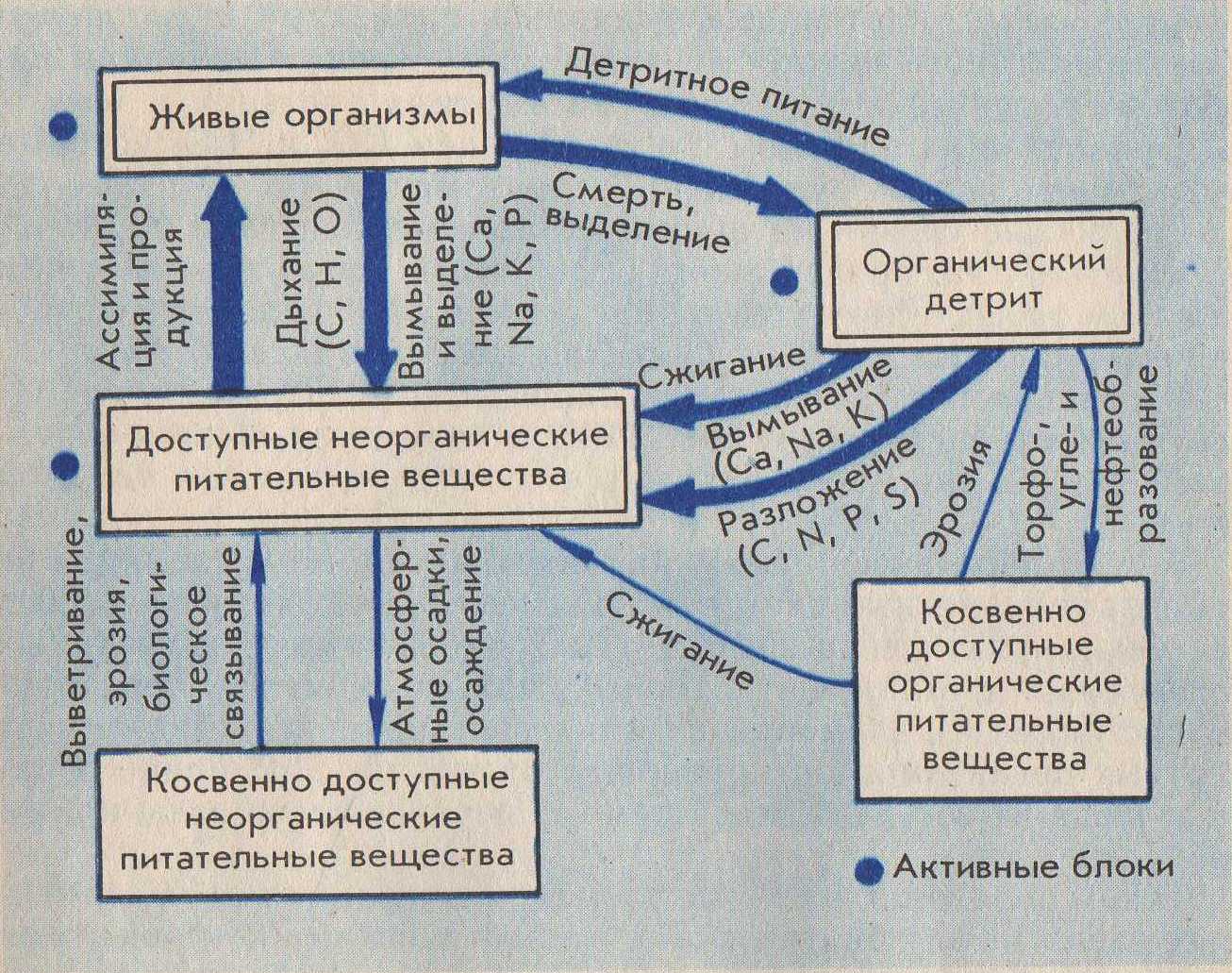 ПРИЛОЖЕНИЕ 3 ПРИЛОЖЕНИЕ 3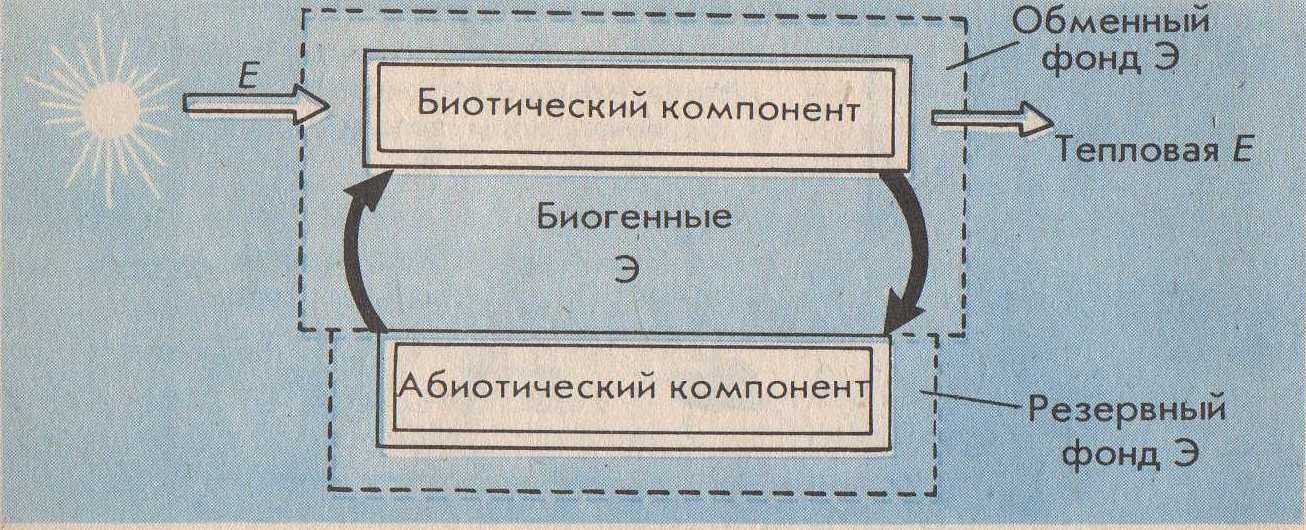 ПРИЛОЖЕНИЕ 3А ПРИЛОЖЕНИЕ 4 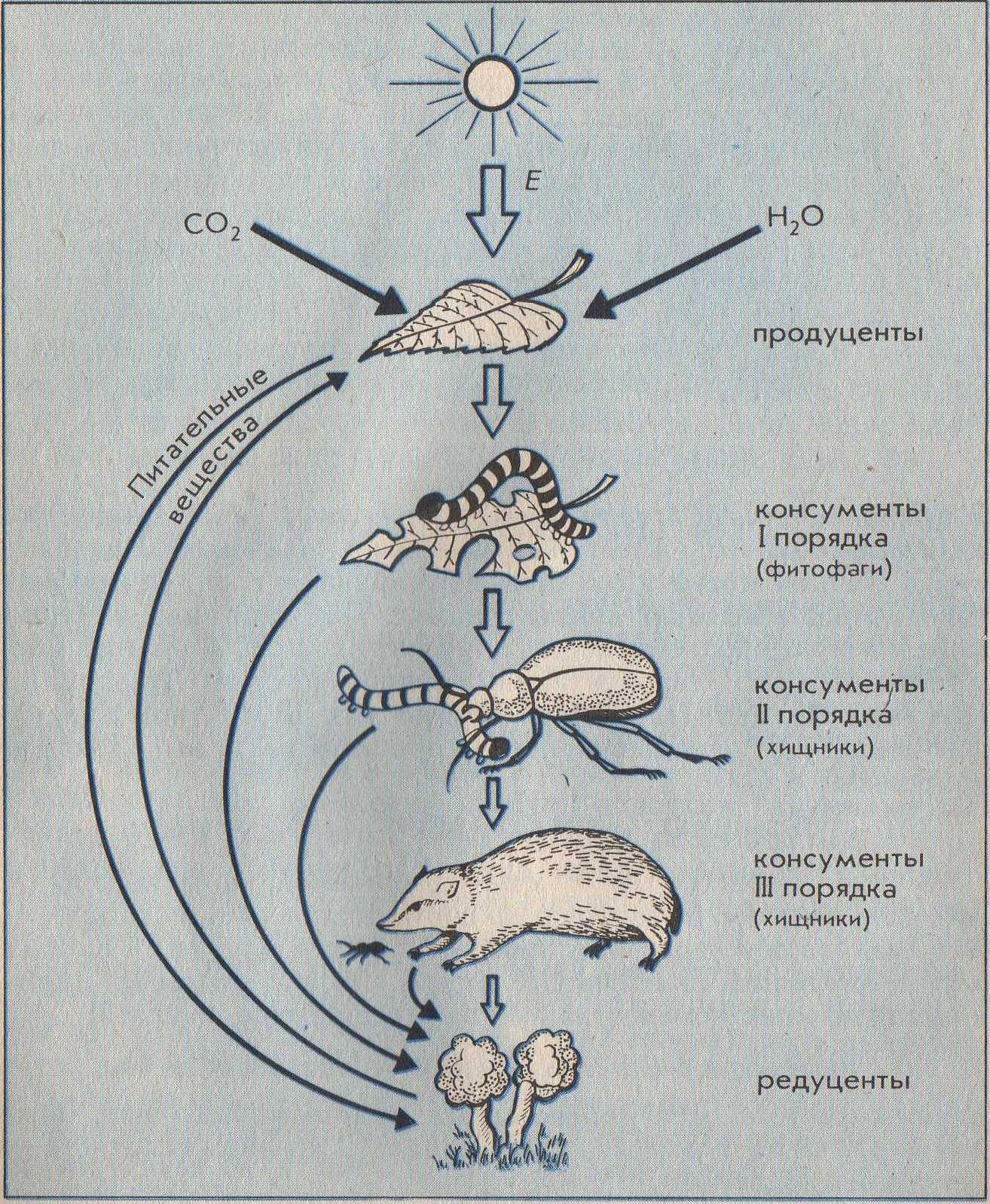 ПРИЛОЖЕНИЕ 4А 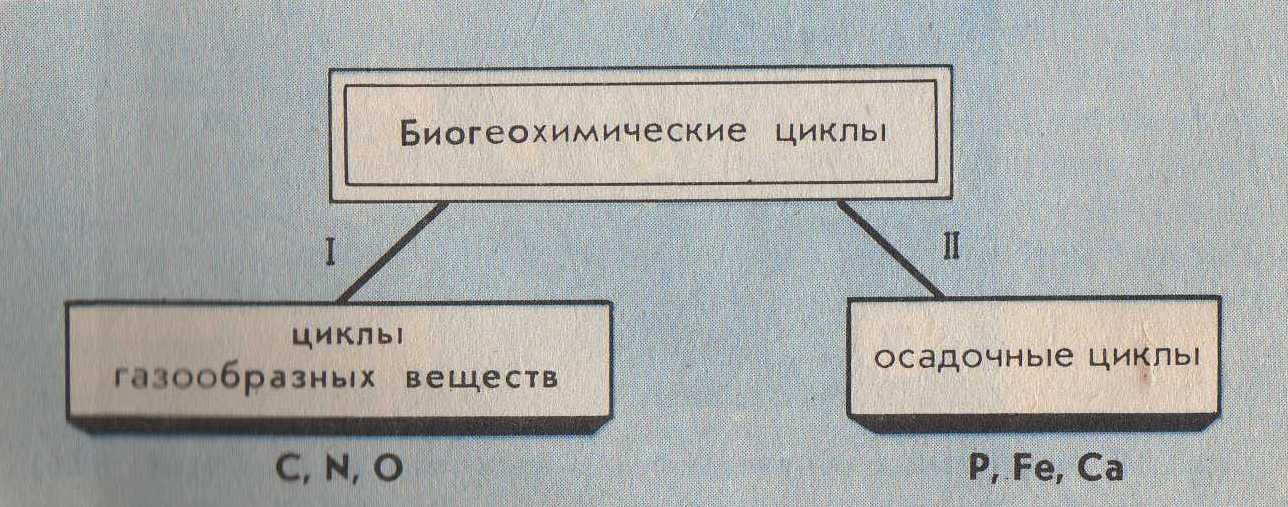 ПРИЛОЖЕНИЕ 5 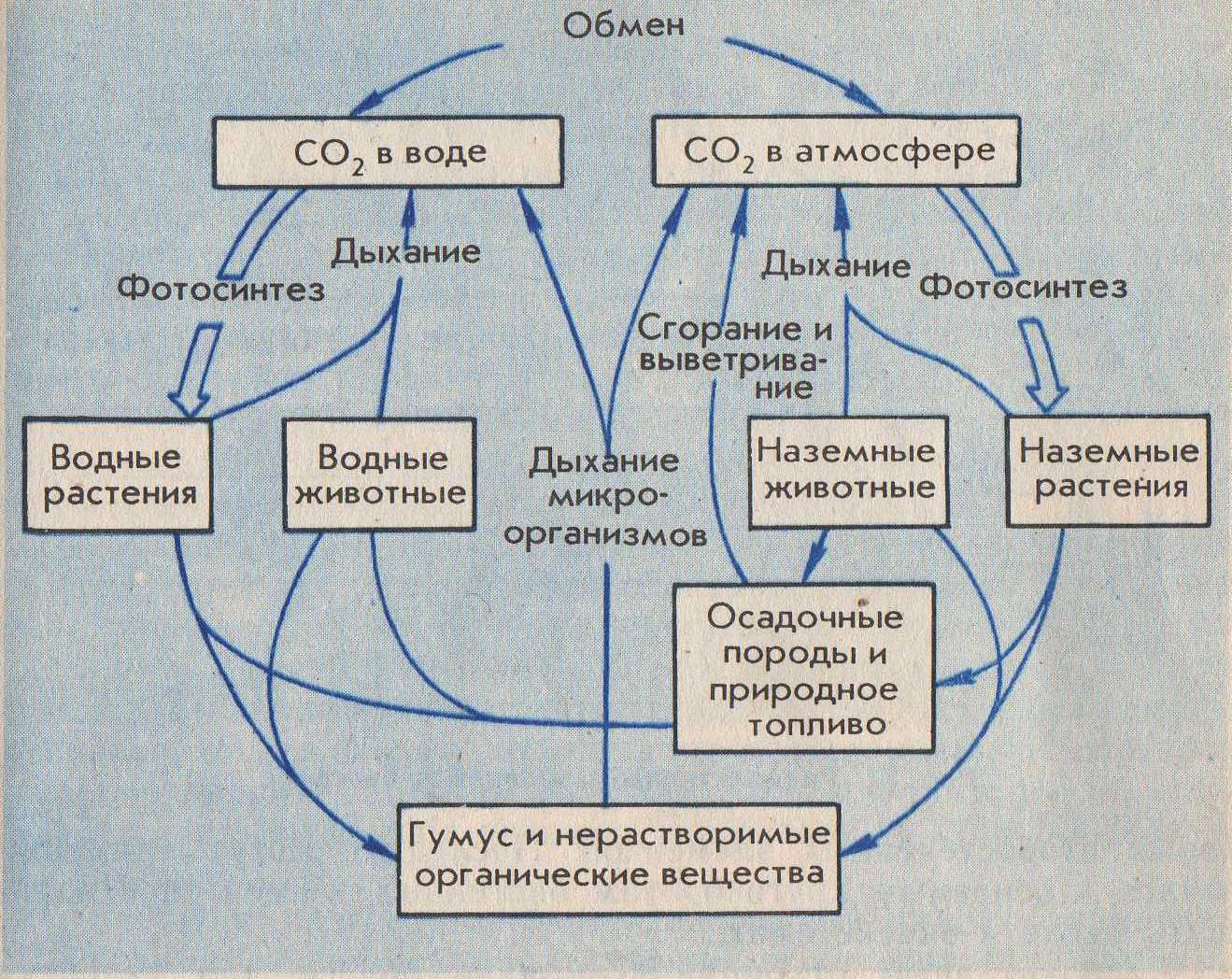 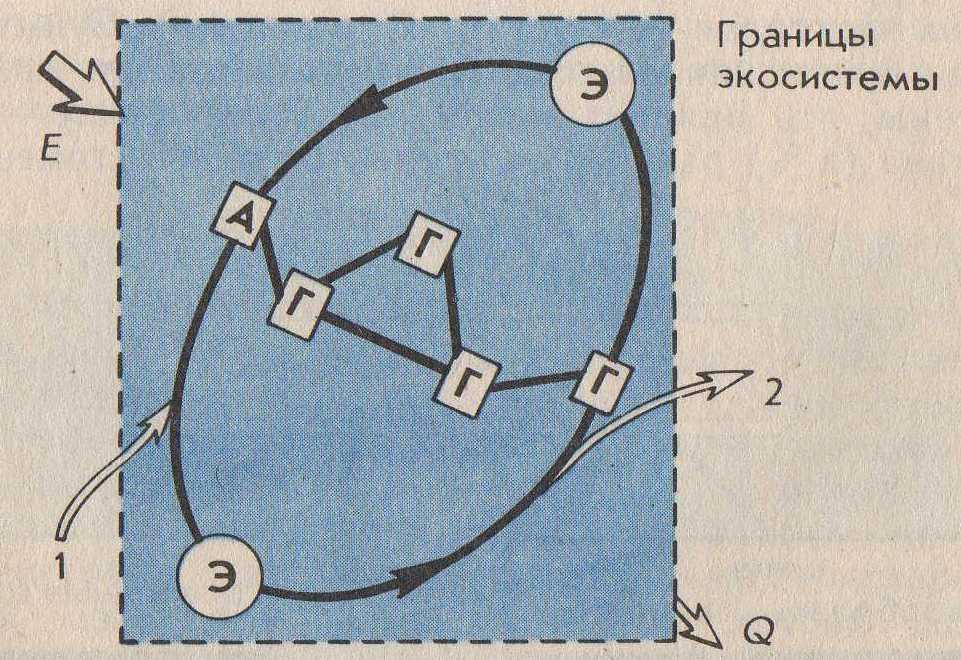 ПРИЛОЖЕНИЕ 5А 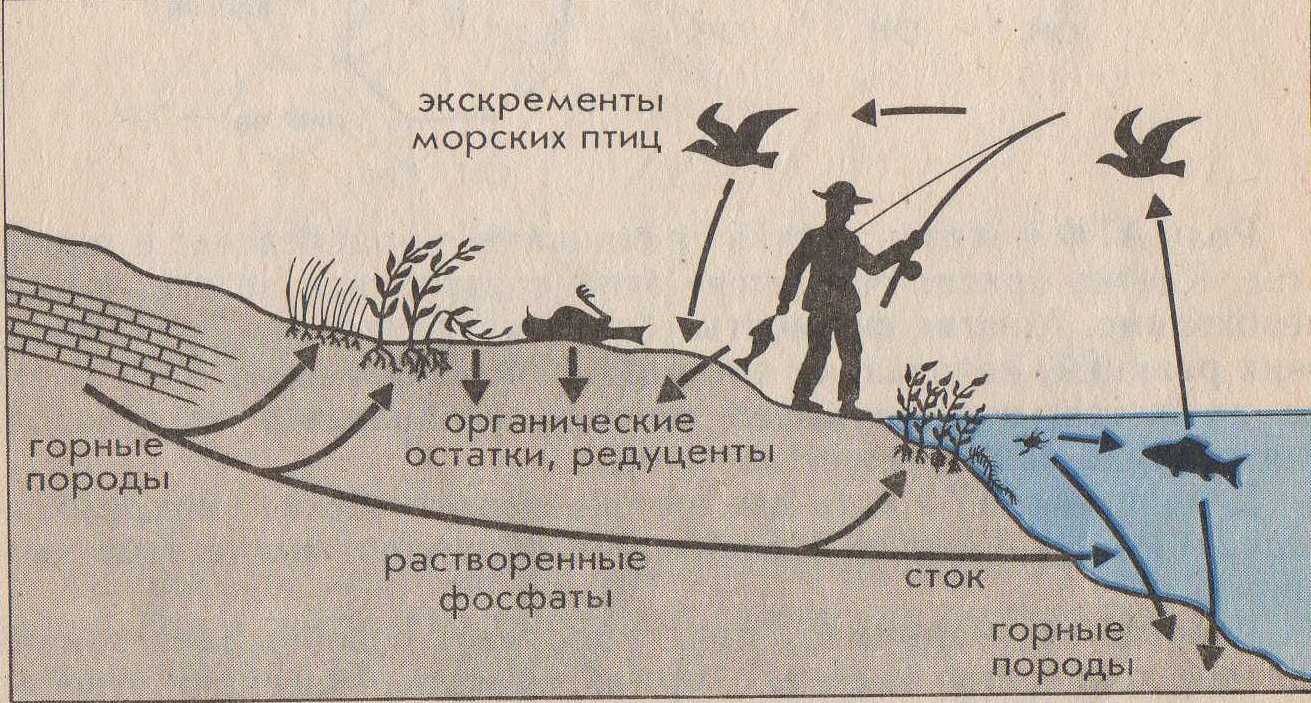 ПРИЛОЖЕНИЕ 6 ПРИЛОЖЕНИЕ 6ПРИЛОЖЕНИЕ 6А 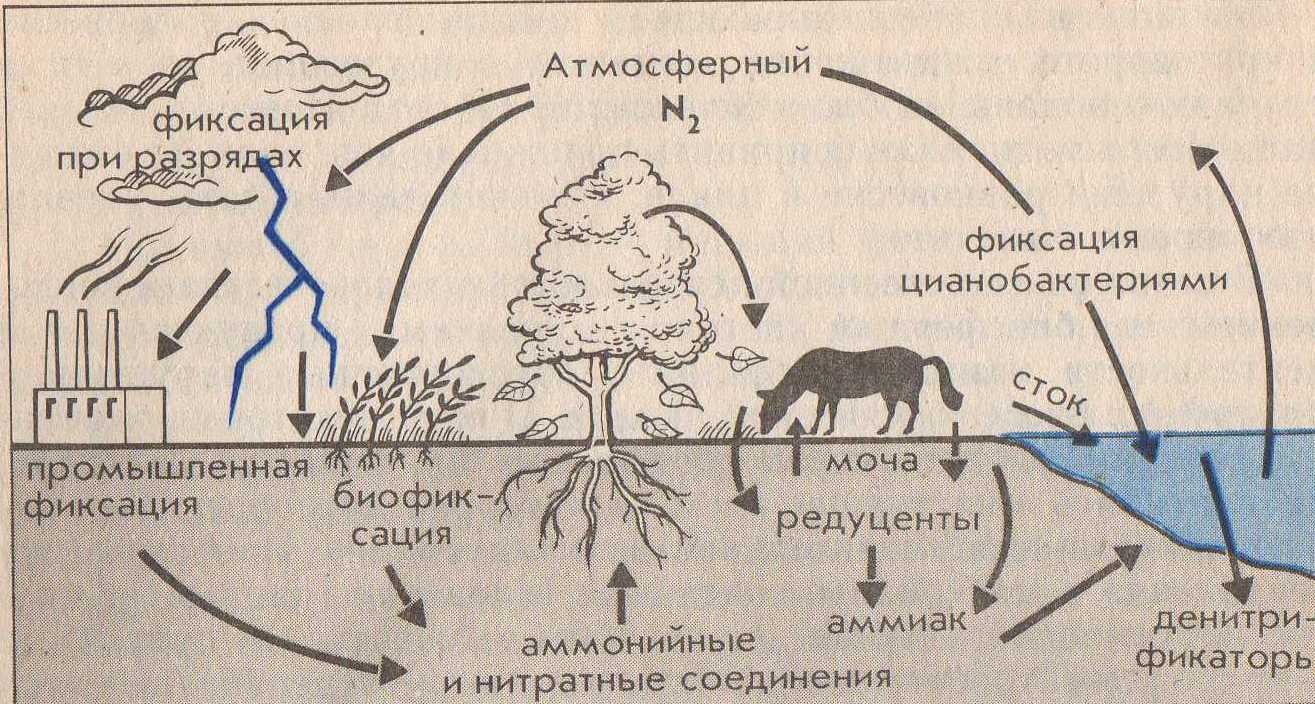 ПРИЛОЖЕНИЕ 7 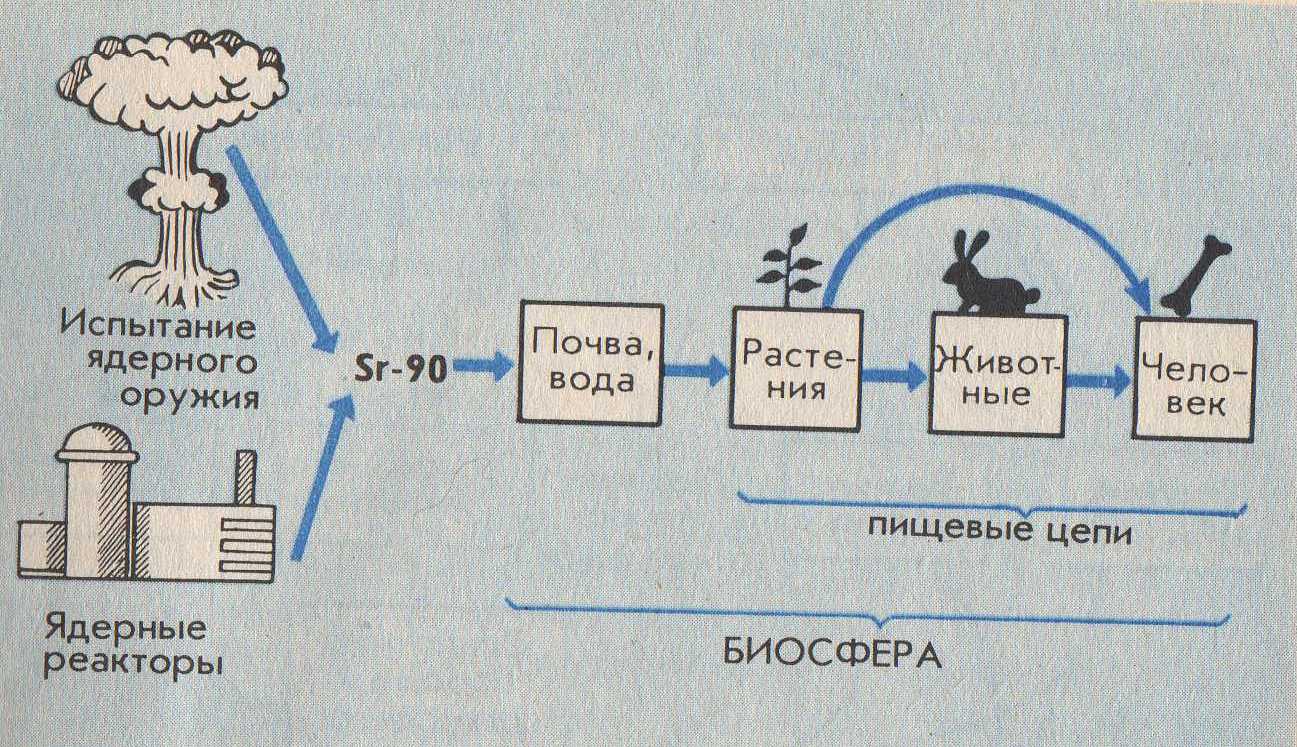 ЛИТЕРАТУРА.
(Шустов С.Б., Шустова Л.В.) М. "Просвещение" 1995г. 2.Экологический словарь юного химика. М., "Педагогика" 1999г. 3."Биохимическая эволюция" (Флоркэн М.) М. Изд-во иностр. литература 1989г. 4. "Биохимическая индикация наземных экосистем" (Подред. Р.Шуберта) М. "Мир" 1988г. 5."Введение в биохимическую экологию" (М.Барбье) М. "Мир" 2000г. 6."Химия – в центре наук". В 2 т. (Браун Т., Лемей Г.Ю.) М. "Мир" 1999г. 7.Интернет сайт www.экология.ru |